免疫缺陷鼠众多,重度免疫缺陷鼠如B-NDG小鼠凭借无T、B、NK 细胞更适合肿瘤造模和免疫重建等实验优势,已在科学家的实验室中崭露头角,各大期刊也不乏它的身影。
B-NDG 小鼠(NOD. CB17- Prkdcscid Il2rgtm1/ Bcgen)在NOD scid 小鼠中敲除了Il2rg 基因,缺乏成熟T、B和NK 细胞(图1A),是目前国际公认的免疫缺陷程度最高的实验小鼠之一,非常适合人源细胞或组织移植,已经成功用于制备CDX、PDX、人PBMC和人CD34+ HSC(造血干细胞)免疫重建等模型,广泛应用在抗体药物或细胞治疗的临床前评价中。使用B-NDG小鼠进行人PBMC或人CD34+HSC免疫重建和肿瘤造模后都能很好地验证抗体药的药效(图1B、1C)。

图 1:(A)B-NDG 小鼠 T 细胞、B 细胞和 NK 细胞缺失;(B)B-NDG 小鼠PBMC重建模型验证CD3/Claudin18.2双抗的药效;(C)B-NDG小鼠CD34+ HSC重建模型验证抗PD-1抗体的药效
但使用B-NDG小鼠进行PBMC和CD34+ HSC免疫重建时也面临着一些问题,如PBMC重建后的T细胞会对小鼠自身细胞进行攻击导致严重的xeno-GvHD反应;CD34+ HSC重建后的NK细胞和髓系细胞重建比例不足。基于这些问题,我们在B-NDG小鼠的基础上开发了多种二代小鼠(表1),以满足特定细胞功能研究和相应靶点药物评价的需求。
表1. B-NDG系列小鼠产品列表

01、B-NDG B2m KO plus小鼠
延长实验窗口期
在敲除B2m基因的同时表达了融合在FcRn基因中的B2m基因,这种小鼠具有B-NDG小鼠的基因背景,同时MHC I类分子表达缺失。抗体在该小鼠与B-NDG小鼠中的代谢没有差异(数据未展示),但可以有效减缓人PBMC重建后诱导的GvHD反应,表现为:小鼠的生存期延长;GvHD反应发生时间延迟;反应的严重程度降低(图2)。
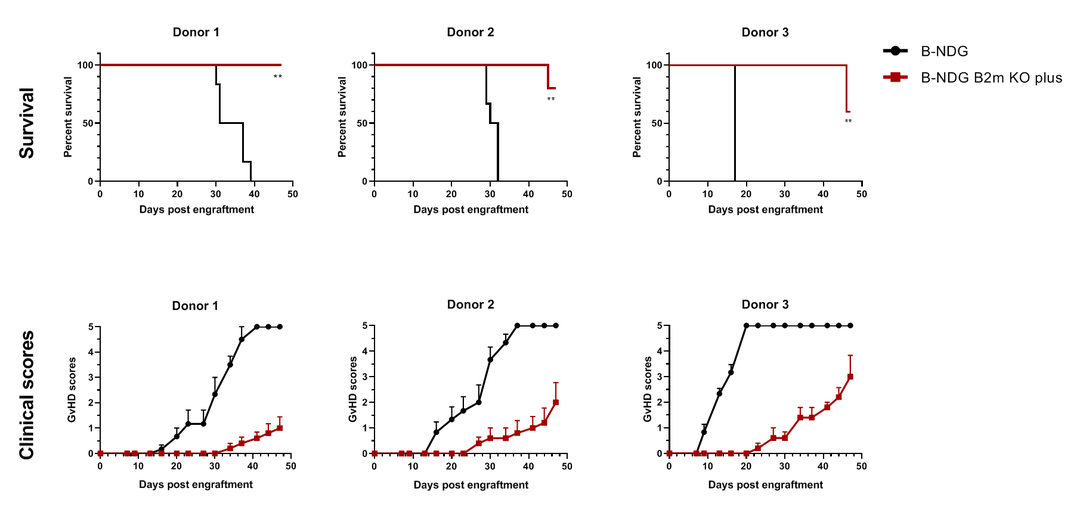
图2:B-NDG小鼠与B-NDG B2m KO plus小鼠的GvHD模型
02、B-NDG hIL-15小鼠
人CD34+HSC重建促进人淋系细胞分化
将人CD34+HSC注射至辐照后的纯合B-NDG hIL15新生鼠的颞静脉,在不同时间点进行内眦采血,并通过流式细胞术分析外周血中T细胞、B细胞和NK细胞的数量与比例。结果显示B-NDG hIL15小鼠成功实现了免疫系统的人源化,重建后的T细胞和NK细胞可以共存,能够满足药效实验的需要(图3)。
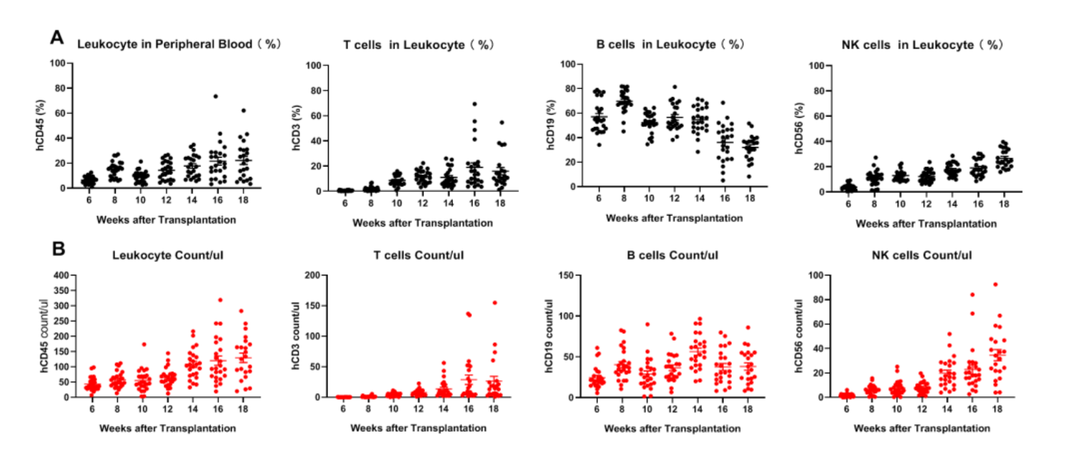
图3:在B-NDG hIL15小鼠中移植人CD34+HSC后各类免疫细胞的流式细胞分析结果 。(A)重建后各免疫细胞的比例;(B)重建后各免疫细胞的绝对数量。
人NK细胞重建促进人NK细胞的增殖与维持
从人PBMC中纯化NK细胞,将其分别静脉注射到B-NDG hIL15小鼠和B-NDG小鼠中,然后使用流式细胞术分析小鼠外周血NK细胞的数量和比例。在注射后2周,与B-NDG小鼠相比,B-NDG hIL15小鼠的外周血中具有更高比例的人NK细胞,并且在注射后的6周仍然可以维持较高的水平。
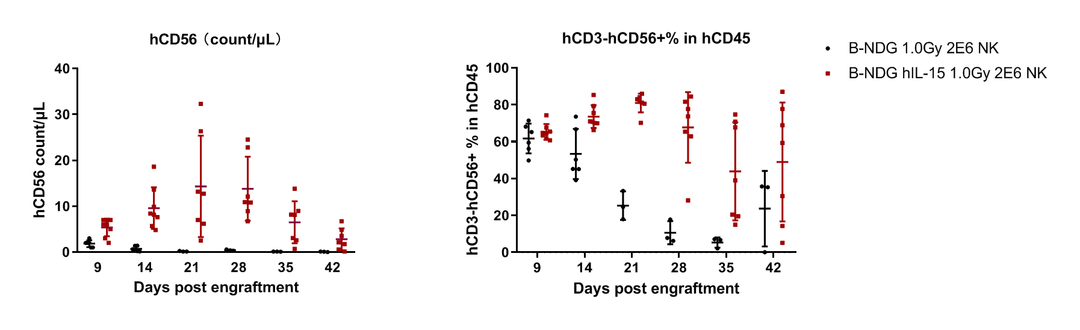

图4:人NK细胞在B-NDG hIL15小鼠中重建后检测各类免疫细胞的比例
03、B-NDG hTHPO mice
无需辐照,进行人CD34+HSC重建
分别在未经辐照的B-NDG hTHPO小鼠和辐照过的B-NDG小鼠中进行人CD34+HSC重建,检测外周血中人CD45+细胞的重建水平并绘制小鼠的生存曲线。结果显示:两种小鼠的人CD45+细胞的重建水平无显著差异,B-NDG hTHPO小鼠的生存率更高,证明使用B-NDG hTHPO小鼠进行免疫重建可以避免辐照对小鼠的损伤(图5)。

图5:未经辐照的B-NDG hTHPO小鼠和辐照过的B-NDG小鼠进行人CD34+HSC重建
04、B-NDG hCSF1/hTHPO mice
无需辐照,促进髓系细胞重建
血液中CSF1是由血管内皮细胞产生的,与各组织局部产生的CSF1可以相互作用,共同调控单核吞噬细胞和破骨细胞的生存、增殖和分化[1]。在未经辐照的B-NDG hCSF1/hTHPO小鼠中进行人CD34+HSC重建后,可以较好的重建人淋系细胞和髓系细胞,特别是单核细胞(图6)。
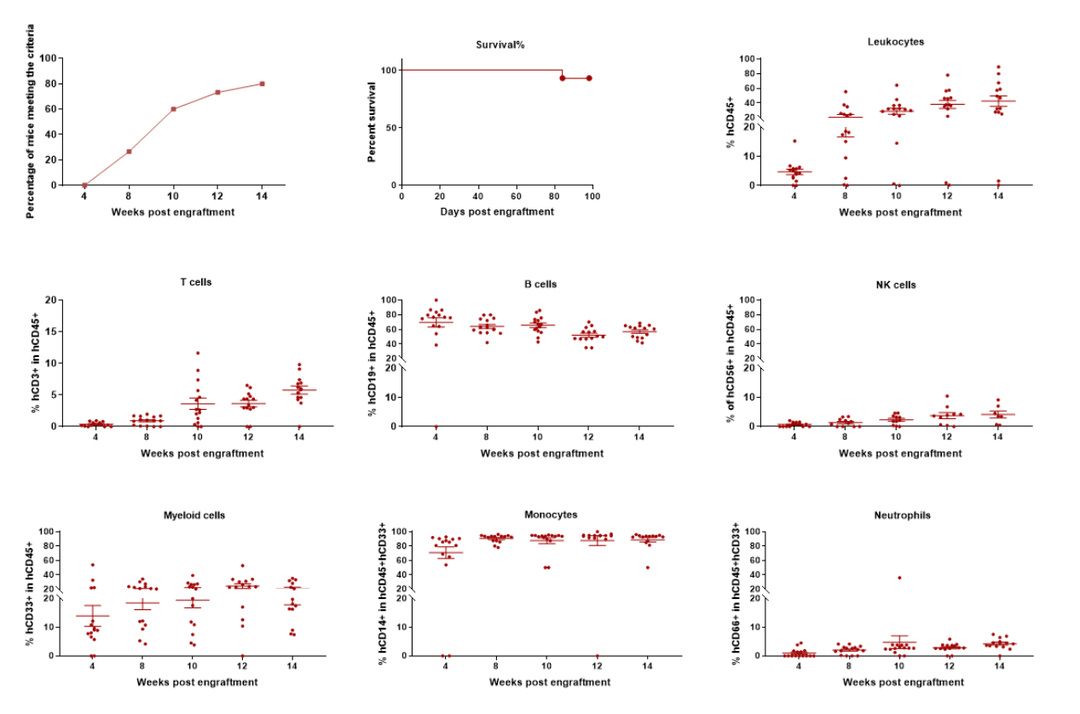
图6:未经辐照的B-NDG hCSF1/hTHPO小鼠进行CD34+HSC重建
想要获取更多B-NDG系列二代小鼠数据吗?赶快拨打电话56967680联系我们进行咨询吧~
参考资料
1. Pixley FJ, Stanley ER. CSF-1 regulation of the wandering macrophage: complexity in action. Trends Cell Biol. 2004;14(11):628-638.






 010-56967680
010-56967680 info@bbctg.com.cn
info@bbctg.com.cn